Konfigurasi elektron adalah susunan elektron-elektron dalam suatu atom atau ion berdasarkan tingkat energi dan orbitalnya, yang menjelaskan sifat kimia dan fisika unsur. Penentuan konfigurasi elektron dilakukan dengan mengisi elektron secara bertahap mulai dari kulit dan orbital energi terendah, mengikuti aturan seperti Prinsip Aufbau, Aturan Hund, dan Prinsip Pengecualian Pauli.
Pengertian dan Tujuan
Definisi:
Konfigurasi elektron merupakan cara penempatan elektron dalam kulit dan subkulit atom atau molekul.
Tujuan:
Untuk memprediksi perilaku dan sifat kimia suatu unsur, menjelaskan pembentukan ikatan kimia, serta memahami struktur tabel periodik.
Dasar-dasar Penulisan Konfigurasi Elektron
Penulisan konfigurasi elektron mengikuti prinsip-prinsip mekanika kuantum dan beberapa aturan kunci:
Prinsip Aufbau:
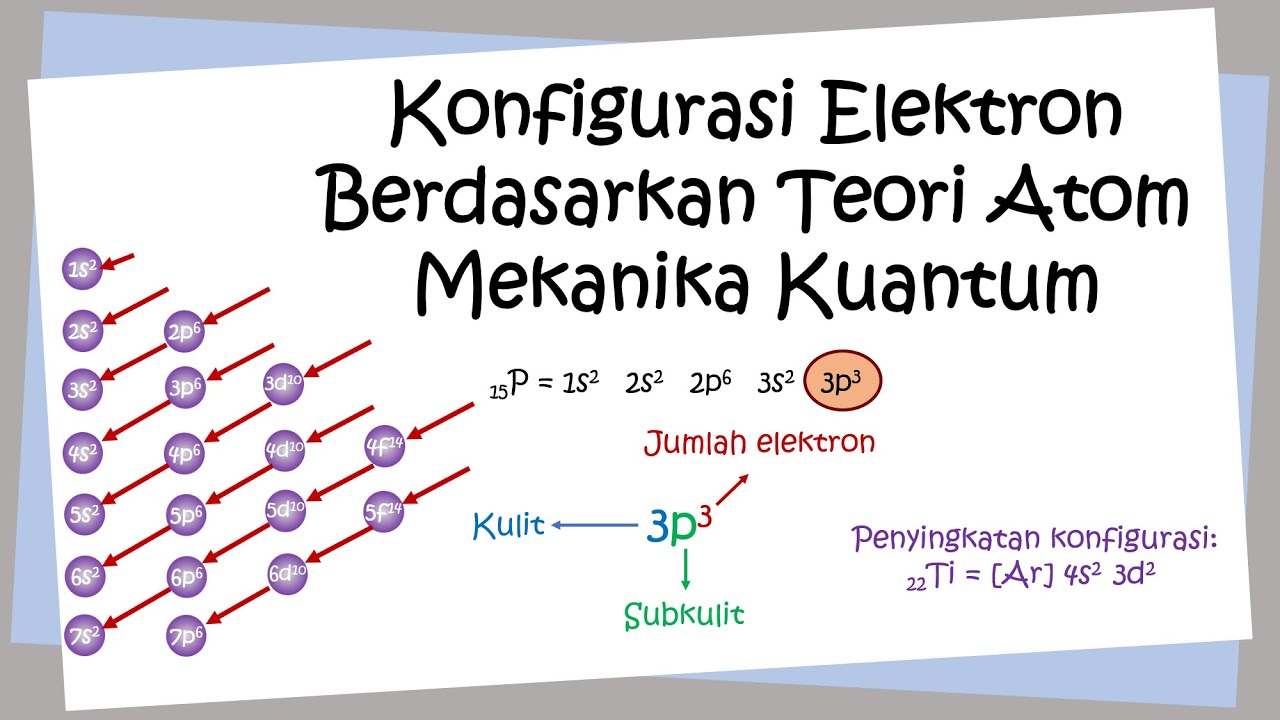
Pengisian elektron dimulai dari tingkat energi terendah ke tingkat energi yang lebih tinggi. Urutan pengisian orbital umumnya adalah 1s, 2s, 2p, 3s, 3p, 4s, 3d, dan seterusnya, seperti yang tertera pada diagram Aufbau.
Aturan Hund:
Dalam suatu subkulit, pengisian elektron akan lebih dahulu terjadi secara tunggal pada setiap orbital sebelum berpasangan, karena elektron akan saling tolak-menolak.
Prinsip Pengecualian Pauli:
Tidak ada dua elektron dalam satu atom yang dapat memiliki keempat bilangan kuantum yang sama. Ini berarti, dalam satu orbital, dua elektron memiliki spin yang berlawanan (satu ke atas dan satu ke bawah).
Jenis-jenis Penulisan Konfigurasi Elektron
Konfigurasi Elektron Kulit:
Susunan elektron berdasarkan kulit atom, misalnya konfigurasi natrium (Na, Z=11) adalah 2, 8, 1.
Konfigurasi Elektron Subkulit:
Menggunakan notasi seperti 1s² 2s² 2p⁶, yang menunjukkan jumlah elektron pada subkulit 1s, 2s, dan 2p masing-masing.
Konfigurasi Elektron Gas Mulia:
Menggunakan simbol gas mulia terakhir yang memiliki konfigurasi elektron stabil, misalnya V (Z=23) dapat ditulis sebagai [Ar] 4s² 3d³.
Contoh
Neon (Ne, Z=10): 1s² 2s² 2p⁶. Subkulit 1s terisi 2 elektron, 2s terisi 2 elektron, dan 2p terisi 6 elektron.
Natrium (Na, Z=11): 1s² 2s² 2p⁶ 3s¹.
Ion Klorida (Cl⁻): Konfigurasi Cl adalah [Ne] 3s² 3p⁵. Karena ion klorida menerima satu elektron, maka menjadi [Ne] 3s² 3p⁶.





















Информация по комментариям в разработке