#infravermelhovibracional,#radiação,#espectroscopianoultravioleta,#vibrações,#transmitancia
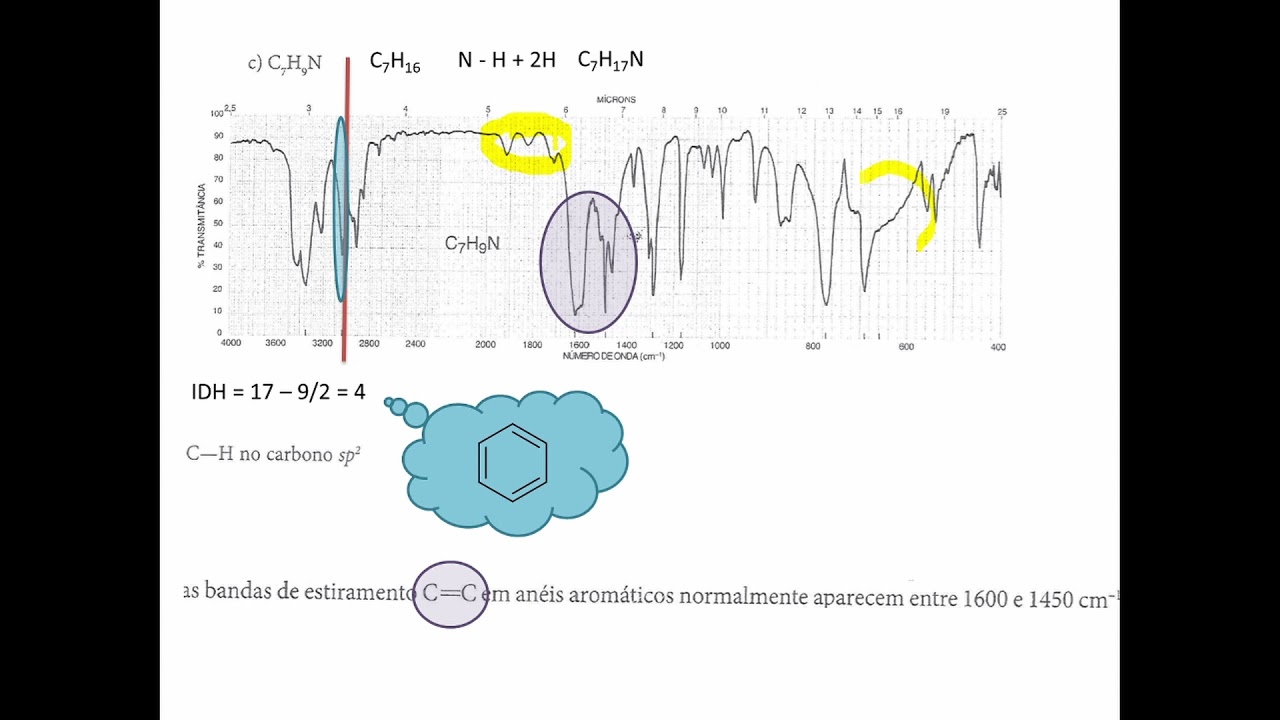
Quase todos os compostos que tenham ligações covalentes, sejam orgânicos ou inorgânicos, absorvem várias frequências de radiação eletromagnética na região do infravermelho do espectro eletromagnético.Essa região envolve comprimentos de onda maiores do que aqueles associados à luz visível, que vão de aproximadamente 400 a 800 nm (1 nm= 10-9 m), mas menores do que aqueles associados a micro-ondas, que são maiores que 1 mm. Na química, interessa-nos a região vibracional do infravermelho,que inclui radiação com comprimentos de ondas (λ) entre 2,5 μm e 25 μm (1 μm = 10-6 m). Apesar de o micrometro (μm) ser a unidade tecnicamente mais correta para comprimento de onda na região do infravermelho do espectro, usa-se o mícron (μ) com mais frequência. Há a relação da região do infravermelho com outras contidas no espectro eletromagnético. A Figura 2.1 mostra que o comprimento de onda λ, é inversamente proporcional à frequência v por meio da relação v = c/λ, em que c = velocidade da luz. Observe também que a energia é diretamente proporcional à frequência: E=hv, em que h = constante de Planck. Desta última equação, pode-se ver qualitativamente que a radiação de energia mais alta corresponde à região de raios X do espectro, onde a energia pode ser grande o suficiente para quebrar as ligações das moléculas. Na outra ponta do espectro eletromagnético, as radiofrequências apresentam energias muito baixas, apenas o suficiente para causar transições de spin, nucleares ou eletrônicos, dentro das moléculas, isto é, ressonância magnética nuclear (RMN) ou ressonância de spin eletrônico (ESR), respectivamente. Existe um resumo das regiões do espectro e dos tipos de transições de energia observadas. Muitas dessas regiões, incluindo a do infravermelho, fornecem informações fundamentais sobre as estruturas de moléculas orgânicas. A ressonância magnética nuclear, que ocorre na região de radiofrequências do espectro, é abordada nos Capítulos 3, 4, 5, 6 e 10, enquanto a espectroscopia no ultravioleta c visível é descrita no Capítulo 7. A maior parte dos químicos refere-se à radiação na região do infravermelho vibracional do espectro eletromagnético em termos de uma unidade chamada número de onda (v), em vez de comprimento de onda (μ ou μm).Números de onda são expressos em centímetros recíprocos (cm-1) e são facilmente computados calculando-se o recíproco do comprimento de onda expresso em centímetros. Para converter um número de onda v em uma frequência v, multiplique-o pela velocidade da luz (expressa em centímetros por segundo). O principal motivo para químicos preferirem número de onda como unidade é que ela é diretamente proporcional à energia {um número de onda maior corresponde a maior energia). Assim, em termos de número de onda, o infravermelho vibracional vai de 4000 a 400 cm-1. Essa faixa corresponde a comprimentos de onda de 2,5 a 25 um. Neste livro, usaremos unicamente número de onda. Em livros mais antigos, podem-se encontrar valores em comprimento de onda. Converta comprimento de onda {μ ou μm) em número de onda (cm-1) usando as seguintes relações:





















Информация по комментариям в разработке