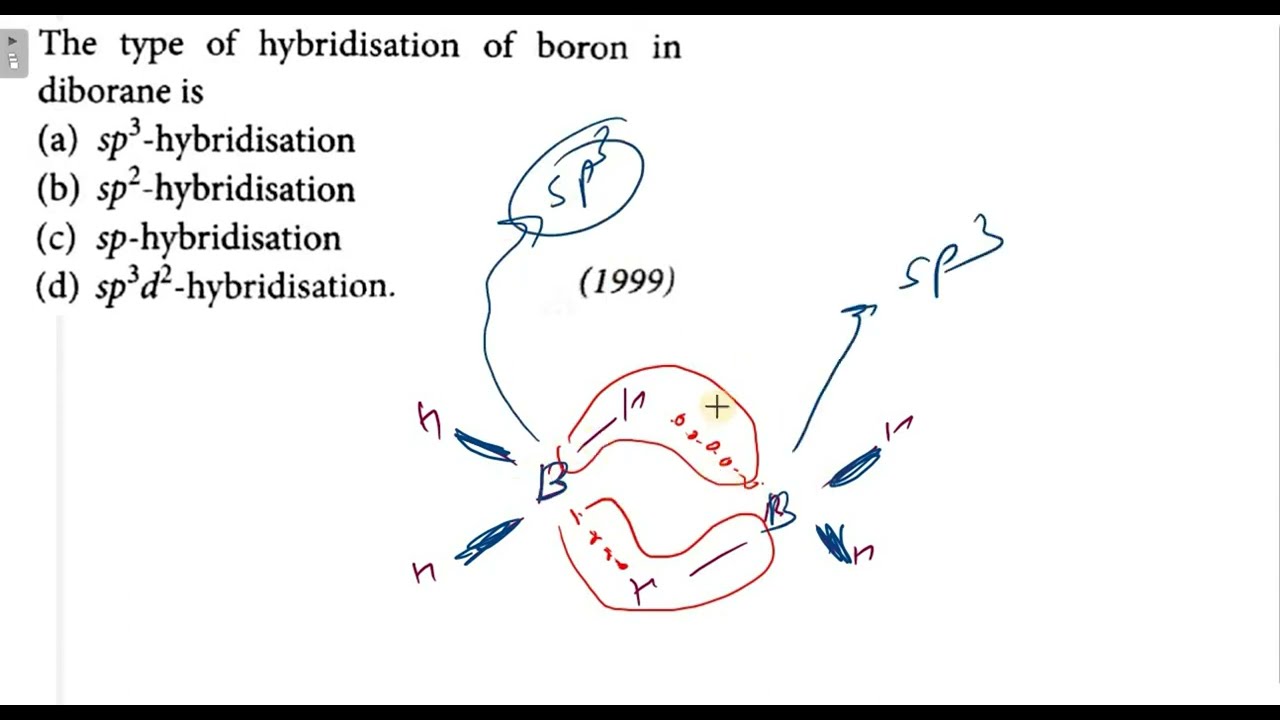
Скачать или смотреть The type of hybridisation of boron in diborane is:
-
2025-06-29
-
151

Скачать The type of hybridisation of boron in diborane is: бесплатно в качестве 4к (2к / 1080p)
У нас вы можете скачать бесплатно The type of hybridisation of boron in diborane is: или посмотреть видео с ютуба в максимальном доступном качестве.
Для скачивания выберите вариант из формы ниже:
-
Информация по загрузке:
Cкачать музыку The type of hybridisation of boron in diborane is: бесплатно в формате MP3:
Если иконки загрузки не отобразились, ПОЖАЛУЙСТА,
НАЖМИТЕ ЗДЕСЬ или обновите страницу
Если у вас возникли трудности с загрузкой, пожалуйста, свяжитесь с нами по контактам, указанным
в нижней части страницы.
Спасибо за использование сервиса video2dn.com
Информация по комментариям в разработке